引言
在半导体工业中,清洁的晶片表面对于电子器件的制造是必不可少的。硅片的表面污染会导致大规模集成电路器件的严重退化。从硅表面去除颗粒最常用的技术是湿化学法,称为RCA清洗的过程。在本文中,我们通过密度泛函理论进行第一性原理计算来研究碱金属溶液中的金属粘附。特别是,研究集中在铝和铁羟基离子的行为上,因为铝和铁通常在APM清洗后在晶片表面大量检测到。目前的理论方法提出了铝和铁羟基络合物粘附过程的反应途径,并提供了反应活化能垒的评估。基于这些计算结果,从硅晶片上金属污染的概率方面讨论了铝和铁之间的差异。本方法的动机是从第一性原理的观点来判断传统的RCA方法,尤其是APM清洗是否能完全防止金属污染。如果APM清洗被认为仍然有希望,那么对pH值的严格控制和温度条件将是重要的。如果没有,则需要补充技术,如添加剂,如表面活性剂和螯合剂,溶液中的金属浓度应显著降低。
实验
使用密度泛函理论进行第一性原理计算。在整个工作中,我们使用了B3LYP方法,为了确定过渡状态和稳定状态,执行了光学优化。含铝金属体系的自旋电子态为单线态,含铁金属体系的自旋电子态为六线态。在几何优化过程中,所有的硅、氧和铝表面原子被允许自由移动,只有终止衬底硅原子的氢原子被固定在它们的初始位置。
铁杂质有两种可能性,即三价铁和四价铁,两种羟基形式的比例取决于溶液的酸碱度。因此,铝(氢)、铁(氢)3和铁(氢)被认为是硅表面金属附着的主要物质。在水溶液中,一些水分子可能作为配体与金属离子结合。因此,知道在这些粘附物质的水性条件下出现哪种配位是非常重要的。进行了初步的优化计算,以显示最稳定和最简单的铝(OH)2、铁(OH)3、铁(OH)4的构型,通过添加水分子来增加金属离子周围的配位,如图1所示。
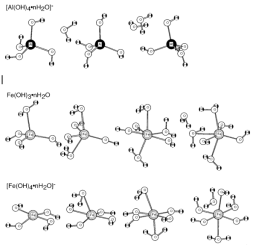
图1 铝或铁羟基配合物的原子构型。通过向具有固定数量羟基的铝或铁金属中添加H2O摩尔数,分别获得了优化的结构
作为铝或铁金属附着到硅表面后的产物,我们假设了一个金属原子通过硅原子之间的一个O原子与硅原子连接的结构。因此,我们重点研究了Si(111)结构中仅包含表面单键的局部部分,即由Si静止原子和第二层中的三个硅原子。
结果和讨论
从能量观点评价反应性。图2、图3和图4所示的反应过程清楚地表明了铝或铁羟基络合物粘附在羟基封端的硅表面上的可能性很大。附着反应总是从金属络合物的羟基官能团和硅表面之间的相互作用开始。因此,反应性是由于羟基的极性。此外,粘附反应产生了H2O分子。这一关键机制常见于三种粘附反应。应该强调的是,根据图2、3和4所示的能量图,反向反应是可能的。硅表面的金属络合物可以在水分子的帮助下被除去。H2O分子首先与硅氧金属连接的氧原子相互作用。随后,H2O分子攻击氧金属键解离。H2O分子的氧氢键的离解导致金属络合物从表面脱离。有趣的是,在铝和铁的情况下,去除反应的能垒都是0.9-1.0电子伏。
图5和图6所示的反应过程提示了通过H2O分子的攻击去除铝和铁络合物的另一种可能性。H2O分子最初与硅氧金属连接的氧原子相互作用。随后,硅氧键溶解被攻击的H2O分子联系在一起。反应的结果是,羟基封端的物质保留在表面,铝(羟基)-或铁(羟基)-3H 0从表面分离。在铝的两种情况下,该反应的势能垒都是1.6电子伏和Fe。因此,与图2、3和4中的逆反应相比,这些反应是不可能的。图5和图6之间势能的显著差异是从产物测量的过渡态的势垒高度。
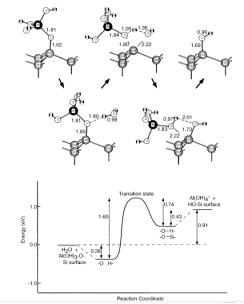
图5 水分子对铝羟基杂质在硅表面的蚀刻反应过程中的原子构型和势能
硅是一种化学惰性材料,生长在硅衬底上的二氧化硅对许多酸溶液是惰性的,即使在高温下也能保持不变。APM溶液在超声波或热加热的辅助下显示出很强的清除颗粒的能力,并且对硅和二氧化硅有微弱的蚀刻作用。HPM溶液可以溶解衬底上除硅以外的大部分金属。因此,只要衬底的基本材料仅使用硅,HPM清洗和APM清洗的组合对于去除金属污染物是非常合理的。然而,这种高清洁能力可能会偶然地导致在最近的先进大规模集成电路技术中存在于衬底上的金属材料的蚀刻。根据目前的理论计算,如果金属溶解在清洗溶液中并形成羟基络合物,原则上不能避免金属污染。应对这种金属污染的措施之一是加入添加剂,以降低清洗液中的金属浓度。
与实验结果的比较。在我们以前的实验研究中,比较了稀HF处理表面和氧化表面之间金属络合物粘附的可能性。在铝、铁和锌的每种情况下,在氧化表面上检测到的金属杂质的量都比在HF处理的表面上检测到的量大得多。从理论计算得到的能量图很好地解释了这一实验结果。
在图1中,随着氢氧化铝周围H2O分子的增加,显示了优化的原子结构。结果表明,不含任何H2O配位的铝(OH)是配合物最基本、最简单的结构单元,铝的配位数为4。同样,我们使用氢氧化铝周围H2O分子的增加。结果,获得了作为基本络合物的Al(OH)3 2H2O,其中三个OH基团组成一个三角形,铝原子以三角形为中心,两个H2O分子排列在三角形的上下。因此,铝原子的配位数为5。这些结果表明,水溶液中复合化合物中金属的配位将敏感地随配体和电荷条件而变化。
总结
量子化学计算阐明了铝或铁羟基杂质附着在溶液中羟基封端的硅表面的反应路径。在铝(OH)—、铁(OH)3·3H2O和[铁(OH)4·2H2O]—粘附的每种情况下,通过硅-氧-氢到的交换产生H2O摩尔电子硅氧金属键合连接。金属粘附的活化能足够小,然后反应在室温下顺利进行。铝或铁羟基杂质的分离也是可能的,这是由于在硅氧金属连接的氧金属或硅氧键处的H2O分子的攻击。氧金属键的离解比硅氧键的离解更有利。然而,与粘附相比,这种分离在能量上是不利的,因此,即使只使用纯水或碱溶液技术对硅晶片进行清洗处理,大部分金属杂质仍会保留在表面上。因此,利用溶液中的添加剂如螯合剂和表面活性剂来防止高酸碱度范围内的金属粘附变得更加重要。
下一篇: 光刻胶中金属杂质对硅基基质的吸附机理